尽管以CAR-T为代表的细胞免疫疗法已在血液肿瘤治疗中取得革命性成功,但其疗效仍受限于T细胞固有的功能瓶颈,如实体瘤浸润困难、抗原逃逸、T细胞耗竭等。为突破这些局限,将CAR工程拓展至其他具有独特免疫生物学功能的效应细胞,构成了下一代细胞治疗的一个重要方向。
2026年04月27日,良渚实验室(科研楼5F区域)/浙江大学医学院附属第一医院黄河教授与胡永仙教授团队,在国际顶级期刊《Nature Reviews Bioengineering》(影响因子37.6)在线发表了题为“CAR-X cell engineering”的综述文章。文章将超越传统T细胞的、经CAR工程化改造的免疫细胞统称为 “CAR-X”。文章提出CAR-X概念,其中“X”可代表自然杀伤(NK)细胞、巨噬细胞(Mac)、调节性T细胞(Treg)等多种免疫细胞平台。本文章系统阐释了CAR-X策略如何通过利用不同免疫细胞的先天优势,设计谱系特异的CAR结构与制造工艺,从而拓展CAR技术在肿瘤及非肿瘤疾病中的治疗前景。
一 CAR-X细胞的免疫生物学优势
CAR-X策略的核心理念在于利用不同免疫细胞谱系特有的免疫功能,弥补传统T细胞的不足,实现“细胞功能与疾病需求的精准匹配”(图1)。其中,CAR-NK具有MHC非依赖性杀伤能力,易于开发通用型、现货型产品,且细胞因子风暴风险较低。CAR-Mac兼具强大的组织浸润、抗原提呈与吞噬清除能力,在重塑实体瘤免疫抑制微环境方面潜力巨大。CAR-Treg作为免疫系统的“刹车”,可靶向特定炎症部位进行精准免疫抑制,为自身免疫病、移植物抗宿主病等提供新策略。CAR-非经典T细胞(如iNKT、γδT和MAIT细胞)兼具先天性与适应性免疫特征,能快速应答、产生多效细胞因子,且同种异体反应风险较低。
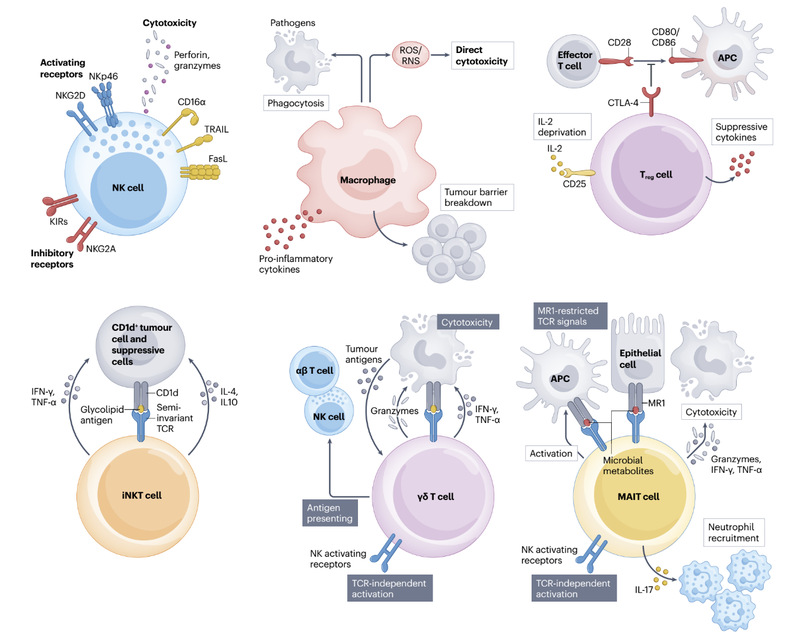
图1. 不同类型CAR-X工程化细胞的功能特征
二 CAR-X细胞的工程化策略
CAR-X的成功转化依赖于谱系特异的工程化策略,涵盖细胞来源、CAR设计、基因编辑与扩增策略(图2)。细胞来源可来自患者自体、健康供体外周血或诱导多能干细胞(iPSC),为规模化生产提供基础。基因工程方面,主要通过病毒转导、mRNA电转或CRISPR等工具导入CAR。关键在于针对不同细胞类型优化共刺激信号域(如NK细胞常用CD28、4-1BB或2B4,巨噬细胞用FcγR)与CAR分子设计。制造工艺需建立稳定、合规的体外扩增与分化体系,确保细胞产品的活性、纯度与可重复性。
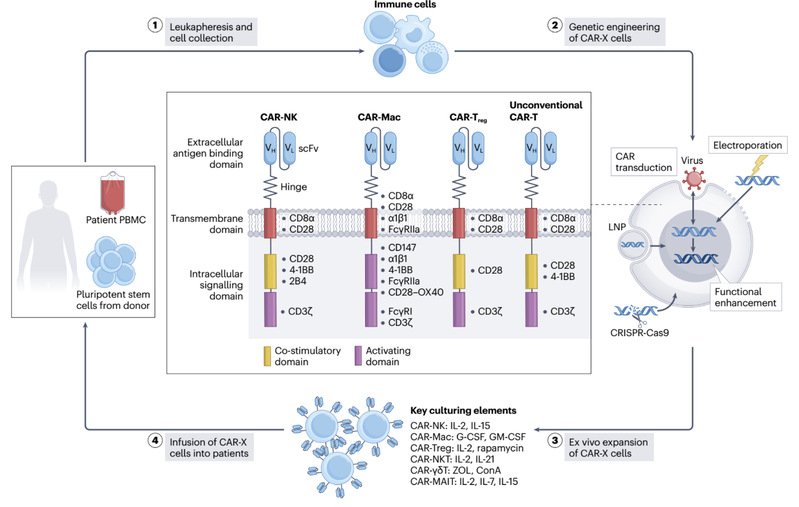
图2 CAR-X细胞的制备流程及其常见结构
三 CAR-X工程化细胞疗法的临床应用
CAR-X平台正推动细胞治疗从血液肿瘤向更广阔领域扩展(图3)。在肿瘤治疗方面,CAR-NK在血液瘤中已展示良好临床可行性;CAR-巨噬细胞与CAR-γδT细胞在实体瘤(如胶质瘤、肝癌)中展现出穿透屏障、克服异质性的潜力。针对非肿瘤疾病,CAR-Treg在1型糖尿病、红斑狼疮等自身免疫病及器官移植排斥的临床前研究中取得突破,实现了靶向、局部的免疫抑制。在安全可控性方面,部分CAR-X细胞(如CAR-NK、CAR-Treg等)自身具有更佳的安全性特性,通过引入可调控的安全开关,进一步为临床应用保驾护航。
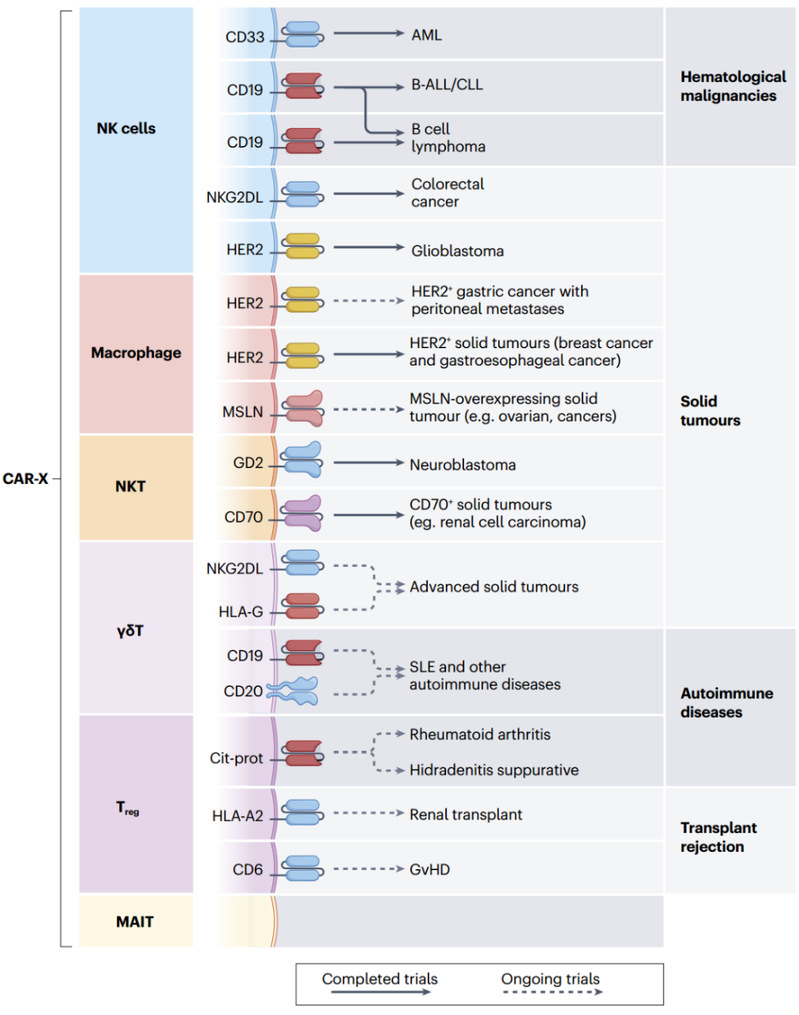
图 3不同CAR-X细胞的治疗应用
总结与展望
CAR-X细胞疗法展现出超越传统CAR-T技术的潜力,尤其在提升治疗安全性、增强实体瘤浸润能力及拓宽适应症范围等方面前景广阔。未来的发展有赖于深入解析各类免疫细胞(特别是稀有的非经典型T细胞)的生物学特性,并建立稳定、可规模化的生产工艺。通过开发细胞类型特异性的CAR设计,有望进一步优化疗效。尽管面临免疫细胞特有的挑战,CAR-X平台仍具备显著优势,未来可整合体内CAR工程(in vivo CAR engineering)等先进策略,以简化生产流程、推动“现货型”疗法落地,进而将CAR技术的应用从血液肿瘤扩展至实体瘤、自身免疫性疾病等更广泛的疾病领域。
(点击左下角“阅读原文”查看论文原文)
招聘
黄河教授和胡永仙教授团队正在积极招聘特聘研究员、博士后和科研助理,欢迎加盟!有意向者请联系李老师(lixia2015@zju.edu.cn),主题注明特聘研究员/博士后/科研助理人员申请。
附浙江大学医学院附属第一医院黄河教授和胡永仙教授团队主要研究方向:1)细胞免疫治疗临床应用和基础研究;2)造血干细胞移植的临床和基础研究;3)干细胞基础和应用研究。

